Contents
まとめ
駆出率が保たれた心不全(HFpEF)では,診断がまず重要
ミミックとされる,アミロイドーシスなどでは治療可能な心不全も多く,適切な診断が重要です
薬剤治療としては,SGLT2阻害薬が治療の中心だと思いますが,各ガイドラインでの推奨度は異なります
肥満があれば,GLP-1作動薬も検討されます
ポピュレーションの観点からは,HFrEFに効果のある薬剤も効果を示す可能性もあるかもしれません
肺動脈圧モニタリングは,早期介入が可能となるかもしれません
今回の論文
心不全
適切な充満圧があるにも関わらず,心臓が代謝組織に十分な酸素供給をできない状態です.
病理学的診断ではなく,臨床症候群であるという点も特徴です.
多くの定義では,主要な症状(息切れ,浮腫,疲労感)を認め,客観的兆候(頸静脈怒張,ラ音,浮腫)を伴います.
これらの定義は,心臓の収縮能(LVEF)とは関係ありません.
駆出率が保たれた心不全(HFpEF)
診断は,呼吸器疾患,虚血性心疾患,高血圧性心疾患,弁膜症,心筋症,アミロイドーシスなど,ミミックとされる病気の除外も必要になります.
加えて心不全兆候を示す事が必要で,運動負荷で超音波所見などの構造上の変化を確認することが必要になります.
現在のガイドラインでは,急性心不全のうっ血を軽減するために利尿療法とSGLT2阻害薬による治療が推奨されています,
SGLT2阻害薬は,入院リスクを現用するために継続投与も推奨されます.
GLP-1作動薬についても,新しい薬剤ですが肥満の軽減と心不全加療の観点から,症状を改善させQOLの改善に寄与することが示されています.
駆出率が保たれた心不全の死亡率を低下させる薬物療法は存在しません.
現在の治療目標は,入院リスクの低減と生活の質の向上になります.
左室機能に応じた分類
LVEFが50%がカットオフとされています.
左室機能軽度低下は,LVEF41-49%になります.
左室機能低下のLVEFは,40%以下とされています.
これらの定義を用いると,心不全で入院する聖人の最大50%はHFpEFということになります.
高齢化や肥満などで,有病率は増加傾向となっています.
HFpEFの病態は複雑で,心臓の廊下や代謝障害など,複数の病態生理学的メカニズムにより引き起こされるとされています.
高齢者や女性に多いのも特徴です.
加えて,HFpEFは,肥満,2型糖尿病,高血圧,心房細動,慢性腎臓病,その他の心血管疾患の有病率が高いとされています.
HFpEFは,多併存疾患が特徴と言えるかもしれません.
HFpEFの死亡リスクは,HFrEFよりも低くなります.
ハザード比0.68,95%信頼区間0.64-0.71
HFpEFの場合,心アミロイドーシスの有病率は6.3%(90歳以上では最大21%)とされており,診断することが極めて重要になります.
診断
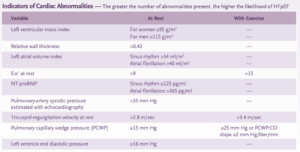
まずは,心エコー検査が簡便で構造的異常の検索にも有用だと思います.
心エコーで,左室拡張不全や左室充満圧上昇などの客観的証拠を検索することになります.
検索・除外として,呼吸器疾患,肥大型心筋症,ファブリー病,心臓アミロイドーシスなどの蓄積・浸潤性疾患などの潜在的な類似疾患の除外が必要になります.
心臓の構造的・機能的異常も重要です.
心不全が疑われる場合は,BNPやNT-proBNPの測定も有用です.
125pg/ml以上のNP-proBNP値の感度は0.98,特異度0.35です.
感度が高値のため,BNPが陰性の場合は心不全ではないと使うことも可能ですが,臨床的には軽度上昇も多く迷うところかもしれません.
労作時呼吸困難感を示す疾患も診断を複雑にさせます.
これらの患者さんの場合は,安静時かつ/または運動中のストレステストにより診断が確定する可能性があります.
心臓MRI検査では,肥大型心筋症や心臓アミロイドーシスなど,HFpEFの類似疾患の除外に役立ちます.
当該論文より引用
治療目標
心不全の兆候と症状に対処し,生活の質を改善させ,入院リスクを減らすことになります.
死亡率を大幅に減らす画期的治療法はありません.
主に支持療法が中心になりますが,以下に薬剤治療介入を記載します.
根本原因と併存疾患の治療
HFpEFの治療戦略の基礎は,心血管・非心血管系の併存疾患(高血圧,心房細動,糖尿病,呼吸器疾患,虚血性心疾患,心臓弁膜症,肥満など)の治療になります.
薬物療法
レニン-アンジオテンシン系阻害薬
CHARM-Preserved試験では,36ヶ月の追跡期間でカンデサルタン(ARB)使用による心血管死亡または心不全入院の複合エンドポイントは有効性を示せませんでした(ハザード比0.89,95%信頼区間0.77-1.03).
しかし,ARBを導入することで心不全入院を減少させました(15% vs 18%, P=0.02).
イルベサルタンを使用したI-PRESERVED試験では,CHARM-Preserved試験と同様の結果が示され,高血圧治療における基地の利点を除けば,HFpEFへの有益な利益は示されていません(複合エンドポイントのハザード比0.95,95%信頼区間0.86-1.05).
ACE阻害薬のペリンドプリルのPEP-CHD試験(慢性心不全高齢者に対するペリンドプリル使用)では,中央値2.1年で,心不全による死亡・入院はプラセボと同様でした(ハザード比0.92, 95%信頼区間0.7-1.21).
ペリンドプリルは1年後心不全入院リスクの軽減とも関連をしていました(ハザード比0.63,95%信頼区間0.41-0.97).
まとめると,心不全治療というよりは高血圧などの併存疾患がある場合は,選択肢に入るという印象でしょうか.
アンギオテンシンネプリライシン阻害薬(ARNi)
PARAGON-HF試験(駆出率が保たれた心不全患者に対するARNiとARBの全般的転帰の前向き試験)では,LVEFが45%を超える心不全感や4822例を対象にARNiが評価されました.
結果は,心血管疾患による死亡または心不全入院の主要評価項目には有意差は認めませんでした(率比0.87,95%信頼区間0.75-1.01).
しかし,女性(率比0.78,95%信頼区間0.59-0.9),LVEFの中央値が57%未満の患者では利益が得られる可能性が示されました(率比0.78,95%信頼区間0.64-0.95).
PARAGLIDE-HF試験(代償不全HFpEFの安定化後にARNIとARBを比較した前向き試験)では,心不全が悪化しLVEFが40%を超えた後に安定した患者466例を対象とし,バルサルタン単独とARNIを比較し,NT-proBNPを低下させました(8周目でNT-proBNPが15%低下,幾何平均値0.85,95%信頼区間0.73-0.1).
特にLVEFが60%未満の患者群で利益が見られました.
しかし,症候性低血圧を犠牲にした結果であり,(オッズ比1.73,95%信頼区間1.09-2.76)安易な導入には慎重になるべきかもしれません.
心不全でLVEFが40%を超える2572例を対象とした,PARALLAX試験(ARNIと併存指間に関連する従来の医療法との生活の質および運動能力との前向き比較試験)では,12週時点でのNT-proBNPの変化を主要評価項目とし,ARNI投与群では標準的な薬物療法(エナラプリルかバルサルタン)またはプラセボ投与群よりも大きな減少が見られました(幾何平均比0.84,95%信頼区間0.8-0.88).
もう1つの主要評価項目である,6分間歩行試験の改善はベースラインから24週までで変化はありませんでした.
まとめると,EFが60%未満,女性では利益を得られる可能性がありますが,症候性血圧低下などに注意する必要があると思われます.
ミネラルコルチコイド受容体拮抗薬(MRA)
Aldo-DHF試験(拡張期心不全のおけるアルドステロン受容体遮断)は,422症例を対象に,1日25mgのスピロノラクトンを投与し,拡張機能,機能特性への影響を調べたPhase2試験になります.
左室重量,ナトリウム利尿ペプチドの減少,拡張機能の改善を認めました.
心不全症状・兆候,QOLへの変化は認めませんでした.
TOPCOAT試験(アルドステロン拮抗薬によるHFpEF治療のPhase3試験)では,LVEF45を超える心不全患者が,スピロノラクトンまたはプラセボを投与されました.
結果は心血管死亡,心停止,心不全入院などの主要評価項目の減少は示されませんでした.
FINEARTS-HF試験(心不全におけるプラセボよりも優れた有効性と安全性を調査するフィネレノン試験)では,LVEF40%以上の患者群で最大40mg/日まで増量すると,主要複合エンドポイントである心血管疾患による死亡等心不全イベント全体の発生率が減少し,駆出率が保たれた心不全患者への使用が裏付けられました.
まとめると,副作用が容認できるのであれば使用は検討され,最大量まで増量することは検討されるのかもしれません.
β遮断薬
HFpEFの最大80%が他の臨床的適応のため,にβ遮断薬を使用しています.
まとめると,HFpEFへの心不全による死亡や入院の現用,生活の質の改善などへの利益は示されていません.
利尿剤
最近までは,根拠が不足しているにもかかわらず,HFpEFに唯一使用される薬剤が利尿薬でした.
ループ利尿剤は,急性心不全の90%で使用されています.
ガイドラインでは,利尿剤を可能な限り低用量で使用し,正常血液量にたっしたら中止することを推奨しています.
高血圧のある患者さんでは,チアジド系利尿剤も選択肢の1つになります.
SGLT2阻害薬
当初は,2型糖尿病に対する治療薬として研究が進められた経緯があります.
その後,心不全にも効果があることが明らかとなってきました.
HFpEFへの効果としては,EMPEROR-Preserved試験(HFpEFの慢性心不全患者におけるエンパグリフロジンの効果)とDELIVER試験(HFpEFの生活改善に向けた効果)の2つの大規模研究がランドマークになっています.
これらの試験では,SGLT2阻害薬はプラセポと比較して,心血管疾患による死亡または心不全による入院の減少というアウトカムを改善させました.
EMPEROR-Preserved試験では,エンパグリフロジンを1日10mg投与し(ハザード比0.79,95%信頼区間0.69-0.9),DELIVER試験ではダパグリフロジンを1日10mg投与していました(ハザード比0.82,95%信頼区間0.73-0.92).
これらの試験の結果を受けて,メタ解析でも一貫した結果を示しています.
現在のガイドラインでは,試験で使用された複合エンドポイントの改善に基づき,HFpEFへのSGLT2阻害薬の使用を推奨しています.
グルカゴン様ペプチドー1受容体作動薬(GLP-1作動薬)
HFpEFの場合は,心臓の代謝異常や糖尿病,肥満の合併が多いのも特徴の1つとされています.
そのため,体重減少や併存疾患コントロールも重要なります.
STEP-HFpEF試験(HFpEFの肥満関連心不全の被験者における週1回のセマグルチド2.4mgの機能と症状に対する効果)であh,プラセポと比較してGLP-1作動薬であるセマグルチド2.4mg週1回の注射により,QOLの改善を認めました.
また,有意な体重減少,運動耐用能の低下も認めました.
心不全におけるセマグルチドに使用は,心血管疾患の重篤なリスク因子(心筋梗塞,心不全,高血圧,脂質異常症)の減少やCRP(炎症)の減少を認めました.
SUMMIT試験では,チルゼパチドの有効性が示されました.
HFpEFおよび肥満の364症例を対照とした,プラセポ対象比較試験になります.
チルゼパチドは,心血管疾患による死亡または心不全悪化の複合リスクの低下(ハザード比0.62,95%信頼区間0.41-0.95)と健康状態の改善(KCCQスコア)を認めました.
まとめとしては,HFpEFと肥満患者への有用性が示されましたがさらなる追試が必要とされています.
治療機器
肺動脈圧のモニタリングにより,早期介入なども検討されています.
CardioMEMSシステムは,肺動脈圧を連続的に測定し,その測定値を医師に送信し,その結果を基に薬物治療の調整を行う方法になります.
550人を対象としたCHAMPION試験(CardioMEMS心臓センサーによるモニタリングでNYHA‐III心不全の転帰を改善)では,LVEFに関係なく薬物治療の最適化により,標準治療と比較して心不全入院が減少しました.
MONITOR-HF試験(慢性心不全348例)では,CardioMEMSによる血行動態モニタリングにより通常治療と比較し,主要評価項目である生活の質(KCCQスコア)の改善が示されました.
不確実な領域
HFpEFという用語は,非特異的表現になります.
任意のLVEFカットオフで心不全を分類していますが,ポピュレーションとしては不均一な集団である可能性があります.
たとえば,肥満などパーソナライズな介入により,特定の薬物治療が走行する可能性は残されているのかもしれません.
また,診断においてもHFpEFのミミックは多数存在するため,除外することが必要になります.
ガイドライン
ガイドラインにより推奨度は異なります.
特徴はSGLT2阻害薬の使用に対する推奨の強さになります.
ESCではClass I推奨ですが,ACC-AHAではIIa, JCS-JHFSでは言及なしとなっています.
本論文のガイドライン推奨の,Table.1はとても見やすいので比較に有用だと思います.